03. Materiais, suas Propriedades e Usos - QUÍMICA
Questão 1
GABARITO E RESOLUÇÃO
GABARITO E
RESOLUÇÃO
O gás liberado é o CO₂ , resultante da decomposição do CaCO₃:
CaCO₃ -> CaO + CO₂
Uma forma de identificar sua presença é reagindo com uma base( Ba(OH)₂ ), já que ele é um óxido de caráter ácido.
Questão 2
GABARITO E RESOLUÇÃO
GABARITO C
RESOLUÇÃO
O Cádmio presente em baterias pode chegar ao solo quando elas são destinadas de forma inadequada, sendo dispostas no ambiente de forma irregular ou incineradas.
O Cádmio tem um elevado potencial de ser tóxico em função de os íons Cd+2 poderem substituir os íons Ca+2 no organismo, causando uma doença degenerativa dos ossos. Isso é possível graças ao raio e a valência dos dois elementos serem de dimensões semelhantes. Além disso, o Cádmio (Cd+2) pode inibir enzimas ativadas pelo Zn+2 e que são importantes para o funcionamento dos rins.
Por isso, é de extrema importância que resíduos que contenham Cádmio, como é o caso das baterias, sejam dispostos de forma adequada. Existem locais específicos que você pode descartar esse tipo de material, basta pesquisar o ponto mais próximo da sua casa.
Questão 3
GABARITO E RESOLUÇÃO
GABARITO C
RESOLUÇÃO
Para resolver esta questão, basta calcular a média ponderada de cada amostra relacionando a porcentagem de Estanho e Chumbo, presentes em cada uma delas.
Amostra I: d=(60*7,3)+(40*11,3)/100=8,9 g/ml
Amostra II: d=(62*7,3)+(38*11,3)/100=8,82 g/ml (atende a norma internacional)
Amostra III: d=(65*7,3)+(35*11,3)/100=8,70 g/ml
Amostra IV: d=(63*7,3)+(37*11,3)/100=8,78 g/ml (atende a norma internacional)
Amostra V: d=(59*7,3)+(41*11,3)/100=8,94 g/ml
Questão 4
GABARITO E RESOLUÇÃO
GABARITO D
RESOLUÇÃO
Para se definir a quantidade de ácido neutralizado é preciso, primeiramente, equacionar a reação:
2 HCL + MG (OH)2 ===> MgCl2 + 2H2O
Isso significa que 1 mol de MG(OH)2 neuraliza 2 Mol de HCL.
Assim, para identificar quantos mol de HCL será neutralizado, basta descobrir quantos mol de MG(OH)2 encontram-se presentes em 9 mL de leite de magnésia. Assim, por regra de 3:
1000 mL_________ 64,8g
9 mL_________x = 0,583 g
A massa molar do leite de Magnésia é de 58,33 g/mol (24,305 (Mg) + (2 x 1,01) (H2) + (2 x 16) (O2) = 58,33 g), sendo assim:
58,33 g ___________ 1 mol
0,583 g ___________ x = 0,01 mol
Assim, considerando a proporção encontrada de 1/2, temos que são neutralizados 0,02 mol de ácido.
Questão 5
GABARITO E RESOLUÇÃO
GABARITO A
RESOLUÇÃO
Considerando a estrutura de

Podemos afirmar que as moléculas X e Y atuam como extratores catiônicos, uma vez que a parte polar da molécula troca íon o H+ pelo cátion do metal.
Questão 6
GABARITO E RESOLUÇÃO
GABARITO A
RESOLUÇÃO
Cgr + 2CuO CO₂ + 2Cu (redução do cobre Cu2+ Cu0; +2 0)
2 . 80 g – 44g
8g – mCO2
mCO2 = 2,2g
Questão 7
GABARITO E RESOLUÇÃO
GABARITO D
RESOLUÇÃO
Como as moléculas desse fármaco são dissolvidas exclusivamente no plasma, que representa aproximadamente 60% do sangue em volume de um total de 5 litros, logo são 0,6 x 5 = 3 litros de plasma. Sendo a concentração máxima de 4 mg/L para que não haja hemorragia, a quantidade máxima de varfarina é de 4 mg/L x 3L = 12 mg. Como a varfarina é administrada por via intravenosa na forma de solução aquosa, com concentração de 3,0 mg/mL, podem ser administrados até 12 mg : 3 mg/ml = 4 ml desse medicamento.
Questão 8
GABARITO E RESOLUÇÃO
GABARITO C
RESOLUÇÃO
O vapor d’água solubiliza os compostos presentes nas folhas, extraindo-os e expondo à sauna.
Questão 9
GABARITO E RESOLUÇÃO
GABARITO A
RESOLUÇÃO
O processo de precipitação é a passagem de algum componente que encontra-se aquoso (dissolvido) para sólido. No caso de ións metálicos, os mesmos, geralmente, se associam à outros íons e passam para o estado sólido. A adição de ácidos minerais evita a precipitação de hidróxidos metálicos de baixa solubilidade, o que poderia subestimar a análise, devido à formação de precipitados (fase sólida), onde se encontrariam uma parte dos metais.
Questão 10
GABARITO E RESOLUÇÃO
GABARITO A
RESOLUÇÃO
Ao amanhecer, ocorrerá o aumento da temperatura, bem como a evaporação dos compostos mais voláteis, como é o caso de alguns óleos essenciais.
Questão 11
GABARITO E RESOLUÇÃO
GABARITO E
RESOLUÇÃO
Baixa solubilidade em àgua
Densidade menor do que a da água
Ponto de fusão igual a – 83°C
Pressão de vapor (conferir na prova)
De acordo com essas características, podemos afirmar que ambas as substâncias são líquidas e imiscíveis.
Dessa forma temos uma mistura heterogênea, sendo assim, podemos utilizar a técnica de decantação para recuperar o acetato de etila. Essa decantação deve ser realizada em um funil adequado, chamado também de funil de decantação.
Questão 12
GABARITO E RESOLUÇÃO
GABARITO D
RESOLUÇÃO
O aumento da velocidade da reação envolvida é devido à maior superfície de contato entre as nanopartículas catalíticas com os reagentes, diminuindo a energia de ativação.
Questão 13
GABARITO E RESOLUÇÃO
GABARITO A
RESOLUÇÃO
A elevação da concentração de dióxido de carbono na água contribui para a formação de cátions H+em solução, ou seja, para a redução de pH (potencial hidrogeniônico).
Questão 14
GABARITO E RESOLUÇÃO
GABARITO D
RESOLUÇÃO
O volume de cada moeda corresponde ao volume de água deslocado na proveta.

A partir das massas fornecidas e dos volumes medidos, pode-se calcular a densidade de cada moeda.
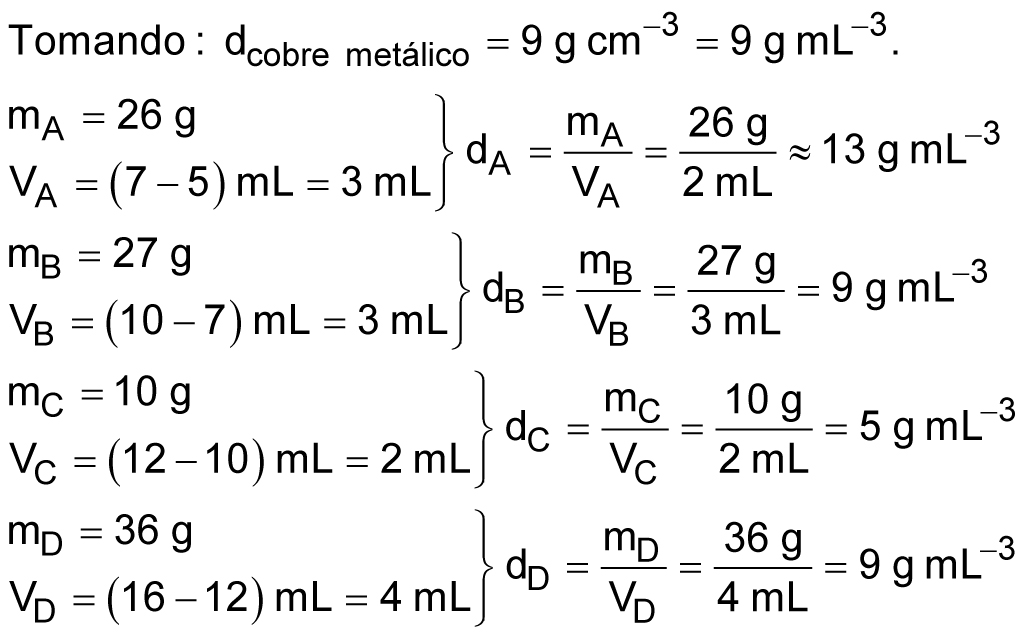
As moedas B e D tem a mesma densidade do cobre metálico (9g cm-3 ou 9g mL-3), logo o investidor adquiriu estas moedas.
Questão 15
GABARITO E RESOLUÇÃO
GABARITO C
RESOLUÇÃO
Os ovos que flutuam são detectados, portanto devem ter densidades menores que a da solução (1,15 g mL-1). São eles: Ancylostoma, Ascaris lumbricoidese Ascaris suum
Questão 16
GABARITO E RESOLUÇÃO
GABARITO D
RESOLUÇÃO
O etanol sobe pelo papel de filtro por capilaridade.